心臟起搏植入裝置感染患者,起搏系統完全移除控制感染期間,需要植入臨時起搏器過渡,但使用球囊漂浮導管以及經股靜脈臨時起搏的方式,保留時間短且併發症高。
近期,北京大學人民醫院昃峰、鄭文成和李學斌等進行的研究表明,對於起搏器依賴患者在感染裝置拔除後,心室主動電極體外臨時持續起搏安全、有效,臨時起搏相關併發症發生率低。
這種臨時起搏方式是在右心室植入主動固定電極,然後連接體表的脈衝發生器,並將脈衝發生器程控為僅雙極模式,作為臨時起搏的橋接。
研究回顧性分析了415例因起搏器感染行電極拔除術且起搏器依賴患者,平均年齡63.8歲,男性占75.9%。這些患者均使用心室主動電極體外橋接臨時持續起搏。
術前在X線指引下首先經股靜脈植入心室四極導管到達右心室心尖部,做臨時起搏備用,完善雙側肘靜脈造影確定雙側鎖骨下靜脈或腋靜脈是否通暢,穿刺前完成囊袋的清創及消毒,並拔除起搏系統,以感染側的鎖骨下或腋靜脈為穿刺入路(對側作為新的永久起搏器植入部位)。
穿刺點避開感染區域且儘量遠離感染切口,同時經穿刺針進導引鋼絲的時候確保鋼絲不通過囊袋空腔,如果肘靜脈造影發現感染側鎖骨下或腋靜脈嚴重狹窄或閉塞,則選擇右側頸內靜脈作為穿刺入路,穿刺成功後沿鋼絲置入7 F可撕開鞘,將永久起搏器使用的心室主動固定電極固定在右心室間隔部。
測試心室電極的阻抗、振幅及閾值,均符合要求後電極導線尾端在體外與再利用的永久起搏器脈衝發生器相連,起搏模式為單腔起搏,雙極起搏、雙極感知,將脈衝發生器固定在患者頸部或者肩部儘量遠離囊袋感染的部位,撤出股靜脈入路的四極心室電極。
415例患者中,臨時起搏電極入路為同側鎖骨下或腋靜脈315 例(75.9%),右側頸內靜脈入路 100例(24.1%)。僅需要植入右心室間隔部臨時起搏電極 405 例(97.6%),採用右心耳+右心室間隔部雙腔體外臨時起搏模式 10 例(2.4%)。
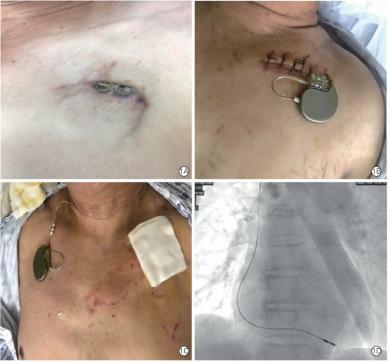
註:1A:為囊袋破潰、感染;1B:經感染側腋靜脈入路心室主動電極橋接體外起搏器;1C:經右側頸內靜脈入路心室主動電極橋接體外起搏器;1D:正位X線下心室主動電極臨時起搏植入右心室低位間隔
圖1囊袋感染及橋接起搏器
臨時起搏電極保留時間為15.3±11.6天,新的起搏器植入後,臨時起搏電極被移除,臨時起搏器起搏閾值、感知靈敏度及電極阻抗均在正常範圍內。
4 例出現與臨時起搏相關的併發症:2例出現電極脫位,予以立即復位;1 例出現穿刺同側腋靜脈入路的部位局部紅腫伴膿性滲出,改穿刺右側頸內靜脈後紅腫逐漸消退;1例同側鎖骨下靜脈入路臨時起搏橋接過程中新出現發熱、血培養陽性,拔除臨時起搏電極改右側頸內靜脈入路後 24小時內體溫恢復到正常,血培養轉陰。
80%的患者隨訪超過1年,中位隨訪24.5個月期間,1 例患者再次出現起搏器感染。不過這1例患者在拔除感染裝置再植入4年後發生再次感染,但是前後兩次感染所培養出的細菌完全不同,這表明第二次感染可能獨立於第一次感染,屬於孤立性事件。
作者表示,對於起搏器依賴的患者而言,起搏電極的脫位會引起很大風險,傳統的臨時起搏器電極脫位率可高達14.3%,而當前研究僅為 0.5%。
心室主動固定電極導線頭端為螺旋電極,體外連接永久起搏器,保證了臨時起搏系統的穩定性,極大地降低了電極脫位的風險。同時由於患者下肢無需制動,下肢靜脈血栓形成風險也大大降低。
研究者指出,在橋接起搏器之前,所有患者均先完善雙側肘靜脈造影,以評估感染側鎖骨下或腋靜脈情況,如發現感染側穿刺靜脈嚴重狹窄或閉塞,則選擇右側頸內靜脈作為橋接臨時起搏電極入路。
不過主動固定電極臨時起搏基本操作相對複雜且費用偏高,研究者認為其主要適用於起搏器完全依賴且需要長時間起搏的患者,但是長時間右心室起搏可引起心室內失同步,對於短時間的臨時起搏,傳統的臨時起搏方式仍為首選。
此外,據介紹,該中心每年有上百台感染裝置被拔除,大多數患者的起搏器功能和電量均處於較好的狀態,對於這些起搏器會在充分的消毒滅菌後再利用。
之前該中心進行的研究表明再植入充分消毒原起搏器與植入新起搏器的患者在長達3.52年的隨訪過程中,再感染發生率相似。
415例患者中,310例局部囊袋感染,75例存在菌血症、30例發生感染性心內膜炎、185例有病態竇房結綜合徵,30例存在高度或完全性房室阻滯。
在感染裝置中,單腔起搏器105 例(25.3%),雙腔起搏器 225 例(54.2%),單腔植入型心臟轉復除顫器 65 例(15.7%),雙腔植入型心臟轉復除顫器20例(4.8%)。

轉載: 請標明「中國循環雜誌」